Ηλεκτρόλυση νερού
Ηλεκτρόλυση νερού με ηλεκτρολύτη
Οι αντιδράσεις που λαμβάνουν χώρα είναι:
Ομως, τα ιόντα
Ο όγκος του
Ηλεκτρόλυση νερού με ηλεκτρολύτη
Οι αντιδράσεις που λαμβάνουν χώρα είναι:
οι οποίες μας δίνουν το συνολικό μηχανισμό της ηλεκτρόλυσης
ΟΞΕΙΔΟΑΝΑΓΩΓΗ
ΚΥΡΙΟΤΕΡΑ ΟΞΕΙΔΩΤΙΚΑ
Στοιχεία Οξειδωτικά στοιχεία είναι τα αμέταλλα τα οποία έχουν την ακόλουθη σειρά οξειδωτικής ισχύος:
F2, Ο3, Cl2, Br2, Ο2, I2, S
Δηλαδή το Cl2 είναι πιο οξειδωτικό από το Br2.
ΚΥΡΙΟΤΕΡΑ ΑΝΑΓΩΓΙΚΑ
Στοιχεία Μέταλλα Η σειρά αναγωγικής ισχύος των μετάλλων σε σχέση με το υδρογόνο είναι: K, Ba, Ca, Na, Mg, Al, Mn Zn, Cr, Fe, Co, Ni, Sn, Pb, H2, Bi, Cu, Hg, Ag, Pt, Au
Διάφορα πειράματα
Συρρίκνωση πλαστικού μπουκαλιού
Προσθέστε σε ένα μεγάλο πλαστικό μπουκάλι
Στη συνέχεια προσθέστε 1 κουταλάκι αποφρακτικό μπάνιου (διάλυμα
Η δέσμευση του
Λιμονένιο και απλές ιδιότητες
Η φλούδα των εσπεριδοειδών περιέχει διάφορες ουσίες. Μία από αυτές είναι και το λεμονένιο ή λιμονένιο με μοριακό τύπο
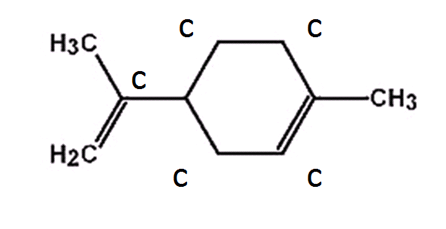
Πείραμα 1ο- Καύση λεμονένιου Ανάψτε ένα κεράκι και πιέστε τη φλούδα του πορτοκαλιού ή του λεμονιού κοντά στη φλόγα με πολύ προσοχή. Παρατηρήστε την αύξηση στην ένταση της φλόγας
Πείραμα 2ο- Σκάσιμο μπαλονιού
Φουσκώστε ένα μπαλόνι. Πιέστε τη φλούδα του πορτοκαλιού ή του λεμονιού κοντά στο μπαλόνι. Παρατηρήστε το σκάσιμο του μπαλονιού.
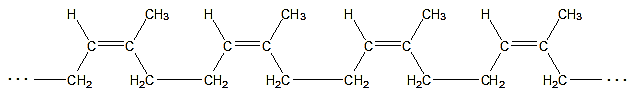
Εξήγηση: Το λεμονένιο είναι ένας κυκλικός υδρογονάνθρακας με μη πολικό χαρακτήρα. Το μπαλόνι αποτελείται από ένα ελαστομερές το cis-πολυισοπρένιο, όπως φαίνεται στην παρακάτω εικόνα που επίσης είναι μη πολικό μόριο. Το αποτέλεσμα είναι το λεμονένιο να διαλύει το ελαστομερές σύμφωνα με τον κανόνα «τα όμοια διαλύουν όμοια», να λεπταίνει η επιφάνεια του μπαλονιού και να σκάει.